Học cỗ môn hoá tới trường 11 thì những em đang được vượt lên thân quen với dạng bài xích tập dượt nhận thấy những hóa học, lúc nào thì hóa học kết tủa, lúc nào thì cất cánh tương đối. Bảng tính tan hoá học tập 11 sẽ gom những em thực hiện được vấn đề này. Bài ghi chép này sẽ hỗ trợ những em nắm rõ vấn đề tuy nhiên bảng tính tan hỗ trợ, phương pháp để ghi ghi nhớ thời gian nhanh và tốt nhất có thể. Bạn đang xem: bảng tính tan lớp 11

Bảng tính tan hoá học tập 11
Học Ngay Hôm Nay - Hóa Thầy Bình Lớp 11
1. Chất tan và hóa học ko tan
- Ví dụ: Cho CaCO3 và NaCl vô ly nước, thì tao thấy chỉ mất NaCl tan còn CaCO3 ko tan.
- Vì vậy đem hóa học ko tan và đem hóa học tan nội địa. Có hóa học tan nhiều và đem hóa học tan không nhiều nội địa. Tan nhiều hoặc không nhiều còn tuỳ vô loại hóa học ví dụ.
2. Định nghĩa chừng tan
- Độ tan là một trong những đại lượng đặc thù cho tới kỹ năng tan của một hóa học bên trên một ĐK chắc chắn.
- Độ tan (S) của một hóa học nội địa là số gam hóa học cơ hòa tan vô 100 g nước sẽ tạo trở thành hỗn hợp bão hòa ở một sức nóng chừng xác lập.
3. Độ tan của một hóa học vô nước
- Nếu 100 gam nước hòa tan:
> 10 gam hóa học tan → hóa học dễ dàng tan hoặc hóa học tan nhiều.
< 1 gam hóa học tan → hóa học tan không nhiều.
< 0,01 gam hóa học tan → hóa học thực tiễn ko tan.
4. Những yếu tố hình ảnh hưởng đến độ tan
Độ tan của một hóa học tùy thuộc vào nhiều yếu ớt tố: sức nóng chừng, áp suất, thực chất của hóa học.
- Với hóa học rắn, tùy thuộc vào sức nóng chừng, thông thường sức nóng chừng tăng thì chừng tan tăng.
Ví dụ: Khi hoà tan lối vô ly nước lạnh lẽo lối tiếp tục tan thời gian nhanh rộng lớn khi hoà tan vô ly nước giá tiền.
- Với hóa học khí, khi tăng sức nóng chừng hoặc hạn chế áp suất thì chừng tan hạn chế.
5. Ý nghĩa bảng tính tan
Bảng tính tan cho tới tao biết, chừng tan những hóa học vô nước: hóa học này kết tủa, cất cánh tương đối, hóa học tan hay là không tồn bên trên vô hỗn hợp. Từ cơ tao rất có thể thực hiện những bài xích nhận thấy và những vấn đề đem kỹ năng và kiến thức tương quan.
Bảng tính tan hoá học tập 11
II. Bảng tính tan hoá học tập 11: Bảng tính tan
1. Bảng tính tan hoá học tập 11
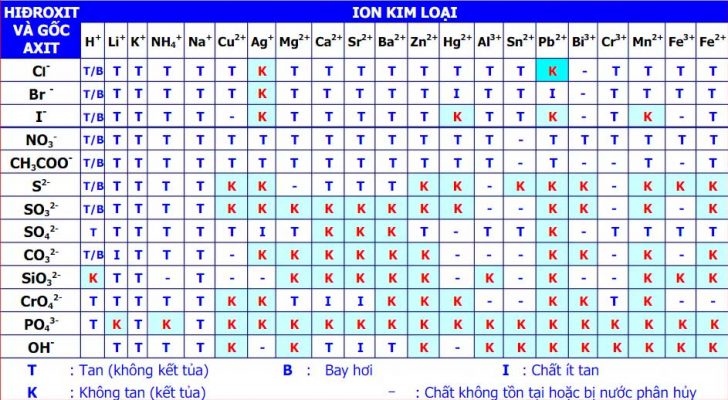
Chú thích:
T: hóa học dễ dàng tan
I: hóa học không nhiều tan
K: hóa học ko tan (ô màu sắc xanh)
B: hóa học cất cánh hơi
- : hóa học ko tồn bên trên hoặc bị nước phân huỷ
Cách gọi bảng tính tan:
Bảng tính tan bao gồm những mặt hàng và những cột. Cột là những cation sắt kẽm kim loại, còn mặt hàng là những anion gốc axit (hay OH-). Với một hóa học ví dụ, tao tiếp tục xác lập ion dương và ion âm, gióng bám theo mặt hàng và cột ứng tao tiếp tục hiểu rằng tình trạng của hóa học cơ bên trên một dù.
2. Cách ghi ghi nhớ bảng tính tan
|
Hợp chất |
Tính chất |
Trừ |
|
Axit (xem ở cột ion H+ và anion gốc axit tương ứng). |
Đều tan. |
H2SiO3 |
|
Bazo (xem ở mặt hàng ion OH- và những cation tương ứng). |
Không tan. |
LiOH, NaOH, KOH, Ca(OH)2, Ba(OH)2, NH4OH. |
|
Muối liti Li+ Muối natri Na+ Muối kali K+ Muối amoni NH4+ |
Đều tan. |
|
|
Muối bạc Ag+ |
Không tan (thường gặp gỡ AgCl). |
AgNO3, CH3COOAg. |
|
Muối nitrat NO3- Muối axetat CH3COO- Xem thêm: cách mở bài nghị luận xã hội |
Đều tan. |
|
|
Muối clorua Cl- Muối bromua Br- Muối iotua I- |
Đều tan. |
AgCl: kết tủa trắng AgBr: kết tủa vàng nhạt AgI: kết tủa vàng PbCl2, PbBr2, PbI2. |
|
Muối sunfat SO42- |
Đều tan |
BaSO4, CaSO4, PbSO4: trắng Ag2SO4: không nhiều tan |
|
Muối sunfit SO32- Muối cacbonnat CO32- |
Không tan |
Trừ muối bột với sắt kẽm kim loại kiềm và NH4+ |
|
Muối sunfua S2- |
Không tan |
Trừ muối bột với sắt kẽm kim loại kiềm, kiềm thổ và NH4+ |
|
Muối photphat PO43- |
Không tan |
Trừ muối bột với Na+, K+ và NH4+ |
3. Màu sắc của một trong những bazơ ko tan hoặc gặp
|
Bazo |
Màu sắc |
|
Mg(OH)2 |
Trắng |
|
Cu(OH)2 |
Xanh lam |
|
Al(OH)3 |
Keo trắng |
|
Zn(OH)2 |
Trắng |
|
Pb(OH)2 |
Trắng |
|
Cr(OH)3 |
Lục xám |
|
Mn(OH)2 |
Hồng nhạt |
|
Fe(OH)2 |
Trắng xanh |
|
Fe(OH)3 |
Nâu đỏ |
Màu của hỗn hợp muối bột tiếp tục bám theo của ion sắt kẽm kim loại.
Xem thêm: she stays incredibly focused and is never distracted by others

Bảng tính tan hoá học tập 11
Bảng tính tan hoá học tập 11 phức tạp rộng lớn đối với bảng tính tan tuy nhiên tao gặp gỡ ở lớp 8 – 9 trước đó. Bảng mang đến 15 mặt hàng 22 cột vì vậy sẽ sở hữu nhiêu dù với khá nhiều hóa học không giống nhau nên cực kỳ khó khăn nhằm ghi nhớ toàn bộ. Vì vậy mong muốn khai quật đảm bảo chất lượng bảng tính tan thì nên cần nắm vững đặc điểm của bộ phận cấu trúc nên phù hợp hóa học và tóm mẹo ghi ghi nhớ nhằm triển khai xong đảm bảo chất lượng những bài xích tập dượt.












Bình luận