Chủ đề công thức tính bộ phận Xác Suất về khối lượng: Công thức tính bộ phận Xác Suất về lượng là 1 trong những khí cụ hữu ích vô hoá học tập và phân tách hợp ý hóa học. Với công thức này, người tiêu dùng rất có thể đo lường và tính toán tỷ trọng lượng của những nhân tố hoặc hóa học vô hợp ý hóa học hoặc láo lếu hợp ý. Việc đo lường và tính toán này chung tất cả chúng ta nắm rõ rộng lớn về bộ phận của hợp ý hóa học và vận dụng trong không ít nghành, kể từ nghiên cứu và phân tích khoa học tập cho tới công nghiệp và hắn tế.
Công thức tính bộ phận Xác Suất về lượng là gì?
Công thức tính bộ phận Xác Suất về lượng được xác lập bằng phương pháp phân chia lượng của một bộ phận cho tới tổng lượng của láo lếu hợp ý, rồi nhân với 100 để sở hữu Xác Suất. Công thức này rất có thể được trình diễn như sau:
Phần trăm lượng = (Khối lượng bộ phận / Tổng lượng láo lếu hợp) x 100%
Ví dụ, nếu như tao sở hữu một láo lếu hợp ý bao gồm 50g hóa học A và 100g hóa học B. Để tính Xác Suất lượng của hóa học A vô láo lếu hợp ý, tao dùng công thức như sau:
Khối lượng A = 50g
Khối lượng B = 100g
Tổng lượng láo lếu hợp ý = 50g + 100g = 150g
Phần trăm lượng A = (50g / 150g) x 100% = 33.33%
Vậy hóa học A lúc lắc khoảng chừng 33.33% lượng vô láo lếu hợp ý.
Bạn đang xem: công thức tính phần trăm khối lượng
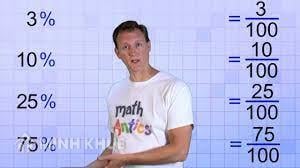
Công thức tính Xác Suất lượng vô một hợp ý hóa học là gì?
Công thức tính Xác Suất lượng vô một hợp ý hóa học là: Phần trăm lượng = (khối lượng mol vẹn toàn tố/khối lượng phân tử của hợp ý chất) x 100%. Để tính Xác Suất lượng, tao cần phải biết lượng mol của nhân tố vô hợp ý hóa học và lượng phân tử của hợp ý hóa học ê. Sau ê, tao phân chia lượng mol nhân tố cho tới lượng phân tử của hợp ý hóa học, rồi nhân thành phẩm với 100 nhằm tính Xác Suất lượng. Ví dụ:
Giả sử tất cả chúng ta cần thiết tính Xác Suất lượng của một hợp ý hóa học sở hữu lượng mol nhân tố là 24g và lượng phân tử của hợp ý hóa học là 120g.
Phần trăm lượng = (24g/120g) x 100% = 20%.
Vậy Xác Suất lượng của nhân tố vô hợp ý hóa học này đó là 20%.
Làm thế này nhằm tính Xác Suất lượng của một hóa học vô một láo lếu hợp?
Để tính Xác Suất lượng của một hóa học vô một láo lếu hợp ý, chúng ta cũng có thể tuân theo quá trình sau:
1. Nhận biết lượng của hóa học cần thiết tính Xác Suất vô láo lếu hợp ý.
2. Xác toan tổng lượng của láo lếu hợp ý.
3. Sử dụng công thức: Phần trăm lượng = (khối lượng hóa học / tổng lượng của láo lếu hợp) x 100%.
Ví dụ, nếu như khách hàng sở hữu một láo lếu hợp ý bao gồm 5g hóa học A và 15g hóa học B, và mình muốn tính Xác Suất lượng của hóa học A vô láo lếu hợp ý, các bạn sẽ thực hiện như sau:
1. Khối lượng của hóa học A là 5g.
2. Tổng lượng của láo lếu hợp ý là 5g + 15g = 20g.
3. kề dụng công thức: Phần trăm lượng của hóa học A = (5g / 20g) x 100% = 25%.
Vậy, Xác Suất lượng của hóa học A vô láo lếu hợp ý này là 25%.
Bước này cần thiết thực hiện trước lúc tính Xác Suất lượng vô một hợp ý chất?
Bước cần thiết thực hiện trước lúc tính Xác Suất lượng vô một hợp ý hóa học là xác lập lượng mol của từng nhân tố sở hữu vô hợp ý hóa học ê. Để thực hiện điều này, cần phải biết công thức chất hóa học của hợp ý hóa học và lượng mol của từng nhân tố tương quan.
Sau Lúc đang được xác lập được lượng mol của từng nhân tố, tao tiếp tục tính tổng lượng mol của những nhân tố vô hợp ý hóa học. Từ ê, tao đã có được tổng lượng của hợp ý hóa học.
Tiếp theo gót, tao dùng công thức tính phần trăm khối lượng, là (khối lượng mol vẹn toàn tố/khối lượng phân tử của hợp ý chất) nhân 100%.
Với quá trình bên trên, tao rất có thể tính được Xác Suất lượng của từng nhân tố vô hợp ý hóa học. Như vậy chung tất cả chúng ta nắm được bộ phận Xác Suất về lượng của những vẹn toàn tử vô hợp ý hóa học.
Tính Xác Suất lượng những nhân tố và tỉ trọng lượng những nhân tố | Hóa học tập trung học cơ sở 89
Tính phần trăm: Video này tiếp tục chỉ dẫn chúng ta phương pháp tính Xác Suất một cơ hội giản dị và hiệu suất cao. Quý Khách tiếp tục biết phương pháp vận dụng tính Xác Suất vô cuộc sống từng ngày, kể từ tính Xác Suất rời giá chỉ vô sắm sửa cho tới tính Xác Suất phát triển vô sale. Đừng bỏ qua thời cơ nâng cao kĩ năng đo lường và tính toán của doanh nghiệp với đoạn Clip này!
Định nghĩa của lượng mol nhân tố là gì?
Khối lượng mol nhân tố được khái niệm là lượng của một mol nhân tố, tức là lượng ứng với số Avogadro của những vẹn toàn tử của nhân tố ê. Đơn vị thông thường được dùng nhằm đo lượng mol nhân tố là gram/mol. Định nghĩa này được chấp nhận tất cả chúng ta đo lường và tính toán Xác Suất lượng của một vẹn toàn tử hay như là 1 nhân tố vô một hợp ý hóa học dựa vào lượng mol nhân tố và lượng phân tử của hợp ý hóa học ê.
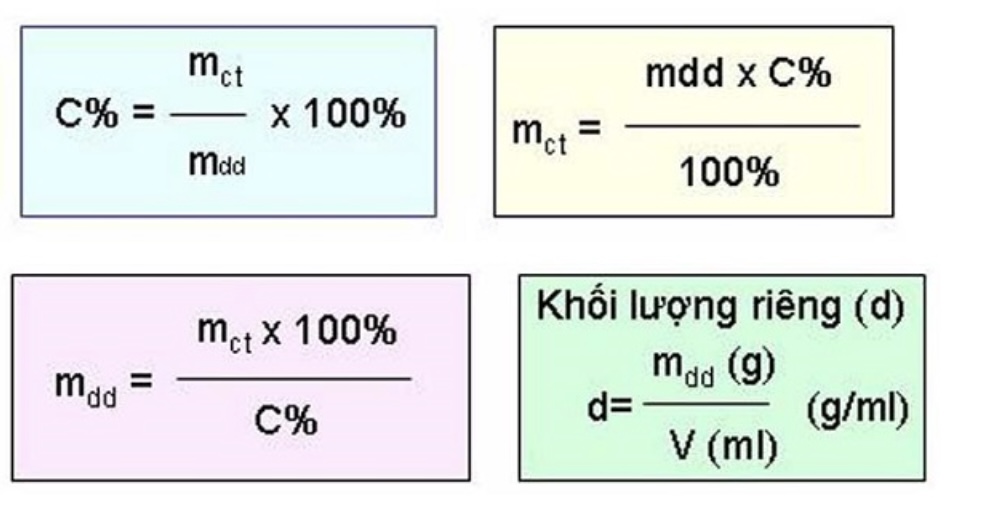
Xem thêm: muốn tính chu vi hình chữ nhật
_HOOK_
Làm thế này nhằm tính lượng mol nhân tố của một chất?
Để tính lượng mol nhân tố của một hóa học, bạn phải thực hiện quá trình sau đây:
Bước 1: Xác toan công thức chất hóa học của hóa học ê. Ví dụ, nếu như mình muốn tính lượng mol của sắt kẽm kim loại Fe (Fe), công thức chất hóa học của chính nó là Fe.
Bước 2: Xác toan lượng vẹn toàn tử của nhân tố ê vô đơn vị chức năng g/mol. Quý Khách rất có thể lần vấn đề này vô bảng tuần trả những nhân tố chất hóa học. Trong tình huống của Fe, lượng vẹn toàn tử của chính nó là khoảng chừng 55.85 g/mol.
Bước 3: Xác toan lượng của hóa học ê vô đơn vị chức năng g. Ví dụ, nếu như khách hàng sở hữu một khuôn mẫu Fe sở hữu lượng là 10 g, thì lượng này được xem là 10 g.
Bước 4: Sử dụng công thức tính lượng mol: Khối lượng mol nhân tố = lượng chất/khối lượng vẹn toàn tử của nhân tố. kề dụng công thức này, tao thu được:
Khối lượng mol nhân tố = 10 g / 55.85 g/mol = 0.179 mol.
Vậy, lượng mol nhân tố của Fe vô khuôn mẫu của doanh nghiệp là 0.179 mol.
Ghi chú: Khi triển khai quá trình này, hãy đáp ứng những đơn vị chức năng của lượng được ghi chép giống hệt vô toàn cỗ quy trình đo lường và tính toán nhằm rời lầm lẫn.
Công thức tính Xác Suất lượng được dùng vô tình huống nào?
Công thức tính Xác Suất lượng (percentage by mass) được dùng nhằm tính tỷ trọng lượng của một bộ phận vô một hợp ý hóa học hoặc láo lếu hợp ý. Công thức này thông thường được vận dụng trong không ít nghành như chất hóa học, hóa sinh, xử lý hóa học thải, và đánh giá unique.
Công thức nhằm tính Xác Suất lượng của một bộ phận vô một hợp ý hóa học là: Xác Suất lượng = (khối lượng của bộ phận / lượng của hợp ý chất) x 100%.
Ví dụ, nhằm tính Xác Suất lượng của một nhân tố vô một hợp ý hóa học, tất cả chúng ta cần phải biết lượng mol của nhân tố ê và lượng phân tử của hợp ý hóa học. Sau ê, tao vận dụng công thức bên trên nhằm tính Xác Suất lượng của nhân tố ê vô hợp ý hóa học.
Chẳng hạn, nếu như tao ham muốn tính Xác Suất lượng của oxi (O) vô hợp ý hóa học H2O, tao hiểu được lượng mol của oxi là 16 g/mol và lượng phân tử của nước là 18 g/mol. kề dụng công thức tính phần trăm khối lượng, tao có: Xác Suất lượng O = (16 g / 18 g) x 100% = 88.89%.
Do ê, công thức tính phần trăm khối lượng được dùng nhằm tính tỷ trọng lượng của một bộ phận vô hợp ý hóa học và vận dụng trong không ít nghành không giống nhau nhằm xác lập bộ phận, đánh giá unique, và nghiên cứu và phân tích những quy trình chất hóa học.

Bài thói quen bộ phận Xác Suất về lượng của đồng vị X vô hợp ý hóa học | Hóa học tập 10
Đồng vị X: Video này tiếp tục tìm hiểu về đồng vị X và những phần mềm đa dạng mẫu mã của chính nó vô khoa học tập và technology. Quý Khách tiếp tục nắm rõ những tính chất và đặc thù của đồng vị X, giống như cơ hội bọn chúng được dùng vô nghiên cứu và phân tích và hắn tế. Hãy nhập cuộc coi đoạn Clip nhằm không ngừng mở rộng kỹ năng khoa học tập của bạn!
Bước ở đầu cuối vô quy trình tính Xác Suất lượng của một hợp ý hóa học là gì?
Bước ở đầu cuối vô quy trình tính Xác Suất lượng của một hợp ý hóa học là triển khai luật lệ tính nhằm đo lường và tính toán Xác Suất lượng dựa vào lượng của hóa học cần thiết xác lập và lượng của láo lếu hợp ý. Công thức công cộng nhằm tính Xác Suất lượng là:
Phần trăm lượng = (khối lượng hóa học / lượng láo lếu hợp) x 100%
Ở trên đây, lượng hóa học là lượng của hóa học cần thiết xác lập (ví dụ: lượng vẹn toàn tố), và lượng láo lếu hợp ý là tổng lượng của toàn bộ những hóa học vô láo lếu hợp ý. Kết trái khoáy sẽ tiến hành đo lường và tính toán bên dưới dạng Xác Suất (%).
Để đo lường và tính toán Xác Suất lượng, tao tiếp tục phân chia lượng hóa học cần thiết xác lập (ví dụ: lượng mol vẹn toàn tố) cho tới tổng lượng của toàn bộ những hóa học vô láo lếu hợp ý, tiếp sau đó nhân với 100%. Kết trái khoáy tiếp tục cho thấy Xác Suất của hóa học cần thiết xác lập vô láo lếu hợp ý theo gót lượng.
Ví dụ, nhằm tính Xác Suất lượng của một nhân tố vô một hợp ý hóa học, tao tiếp tục phân chia lượng mol của nhân tố ê cho tới lượng phân tử của hợp ý hóa học rồi nhân với 100%.
Ví dụ rõ ràng và quá trình cụ thể rất có thể được nhìn thấy trong số mối cung cấp xem thêm chủ yếu thống như sách giáo trình hoặc trang web thường xuyên ngành.
Công thức tính Xác Suất lượng sở hữu phương pháp tính riêng biệt cho tới từng hợp ý hóa học không?
Công thức tính Xác Suất lượng rất có thể sở hữu những đổi thay thể tùy nằm trong vào cụ thể từng hợp ý hóa học. Tuy nhiên, sở hữu một công thức công cộng nhằm tính Xác Suất lượng vô đa số những tình huống. Đó là:
Phần trăm khối lượng= (khối lượng của một trở thành phần/khối lượng tổng) x 100%
Đầu tiên, bạn phải xác lập lượng của một bộ phận vô hợp ý hóa học. Sau ê, tính tổng lượng của toàn bộ những bộ phận vô hợp ý hóa học.
Tiếp theo gót, lấy lượng của một bộ phận vô hợp ý hóa học phân chia cho tới tổng lượng của toàn bộ những bộ phận rồi nhân với 100%. Như vậy tiếp tục cho tới tao Xác Suất lượng của bộ phận ê vô hợp ý hóa học.
Ví dụ, nếu còn muốn tính Xác Suất lượng của sắt kẽm kim loại A vô hợp ý hóa học AB, tao tiếp tục thực hiện như sau:
1. Xác toan lượng của sắt kẽm kim loại A vô hợp ý hóa học.
2. Tính tổng lượng của tất cả sắt kẽm kim loại A và B vô hợp ý hóa học.
3. Lấy lượng của sắt kẽm kim loại A phân chia cho tới tổng lượng và nhân với 100% nhằm tính Xác Suất lượng của sắt kẽm kim loại A vô hợp ý hóa học.
Đây là cơ hội công cộng nhằm tính Xác Suất lượng vô đa số những tình huống, song so với một số trong những hợp ý hóa học phức tạp, rất có thể sẽ sở hữu được những công thức tính không giống phức tạp rộng lớn.
Định nghĩa của lượng phân tử của hợp ý hóa học là gì và thực hiện thế này nhằm tính nó?
Khối lượng phân tử của một hợp ý hóa học là tổng lượng của toàn bộ những vẹn toàn tử vô một phân tử của hợp ý hóa học ê. Để tính lượng phân tử, tất cả chúng ta cần phải biết những lượng vẹn toàn tử của những nhân tố tạo thành hợp ý hóa học ê.
Công thức tính lượng phân tử của hợp ý hóa học được những nhân tố A, B, C,... tạo nên trở thành là:
Khối lượng phân tử = (số lượng vẹn toàn tử A x lượng vẹn toàn tử A) + (số lượng vẹn toàn tử B x lượng vẹn toàn tử B) + (số lượng vẹn toàn tử C x lượng vẹn toàn tử C) + ...
Sau Lúc tính được lượng phân tử của hợp ý hóa học, tao rất có thể tính Xác Suất lượng của từng nhân tố vô hợp ý hóa học theo gót công thức:
Phần trăm lượng vẹn toàn tử A = (số lượng vẹn toàn tử A x lượng vẹn toàn tử A ÷ lượng phân tử) x 100%
Phần trăm lượng vẹn toàn tử B = (số lượng vẹn toàn tử B x lượng vẹn toàn tử B ÷ lượng phân tử) x 100%
Phần trăm lượng vẹn toàn tử C = (số lượng vẹn toàn tử C x lượng vẹn toàn tử C ÷ lượng phân tử) x 100%
và kế tiếp với những vẹn toàn tử không giống.
Ví dụ, nhằm tính Xác Suất lượng của những vẹn toàn tử vô hợp ý hóa học H2O (nước), trước tiên tao cần phải biết lượng vẹn toàn tử của nhân tố oxy (O) và nhân tố hydro (H). Rồi triển khai đo lường và tính toán như công thức bên trên.
Như vậy, nhằm tính lượng phân tử của hợp ý hóa học và những Xác Suất lượng của vẹn toàn tử vô hợp ý hóa học, tất cả chúng ta cần phải biết lượng vẹn toàn tử của những nhân tố tạo nên trở thành hợp ý hóa học.
_HOOK_











Bình luận