Lý thuyết: Sơ lược về bảng tuần trả những yếu tắc hóa học
I. Nguyên tắc bố trí những yếu tắc chất hóa học vô bảng tuần hoàn
- Năm 1869, mái ấm chưng học tập người Nga D. I. Mendeleev tiếp tục kiến tạo bảng tuần trả theo hướng tăng dần dần lượng vẹn toàn tử.
- Các mái ấm khoa học tập tiến bộ tiếp tục chứng tỏ rằng năng lượng điện phân tử nhân vẹn toàn tử mới nhất là hạ tầng nhằm kiến tạo bảng tuần trả.
- Hiện ni, bảng tuần trả những yếu tắc hoá học tập bao gồm 118 yếu tắc được kiến tạo theo dõi nguyên lý sau:
+ Các yếu tắc chất hóa học được bố trí theo hướng tăng dần dần của năng lượng điện phân tử nhân.
+ Các yếu tắc chất hóa học vô và một sản phẩm đem nằm trong số lớp electron vô vẹn toàn tử.
+ Các yếu tắc chất hóa học vô và một cột đem đặc thù chất hóa học tương tự nhau.
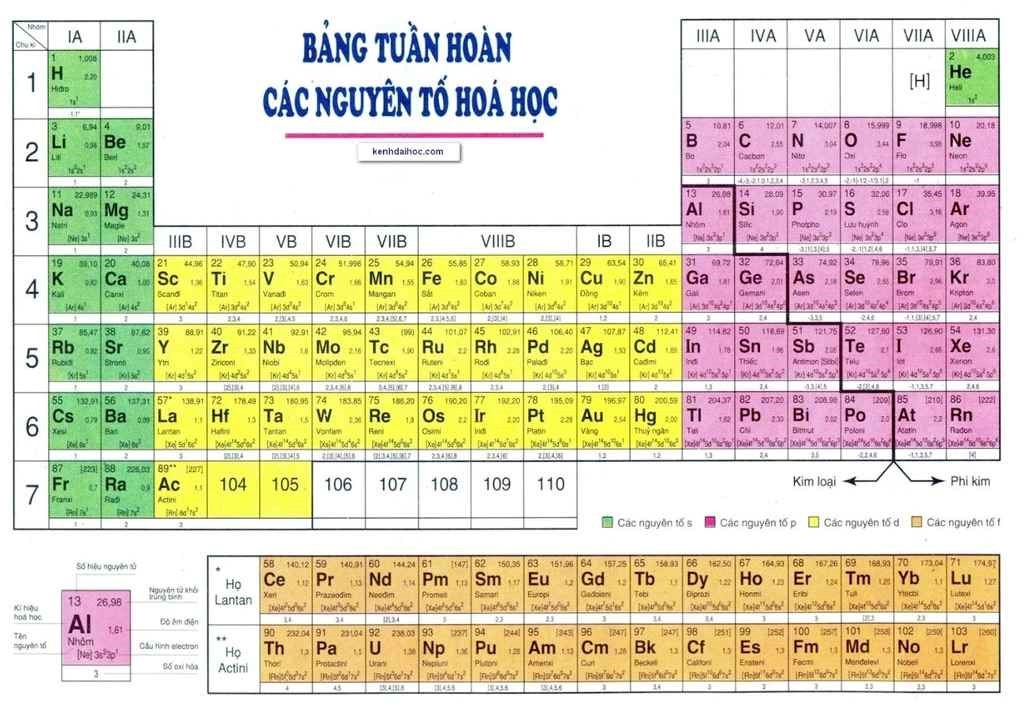
Một kiểu bảng tuần trả những yếu tắc hoá học
II. Cấu tạo ra bảng tuần trả những yếu tắc hóa học
1. Ô vẹn toàn tố
- Mỗi yếu tắc hoá học tập được bố trí vào một trong những dù của bảng tuần trả, được gọi là dù yếu tắc.
Ví dụ 1: Ô yếu tắc carbon cung ứng những vấn đề về vẹn toàn tử carbon.
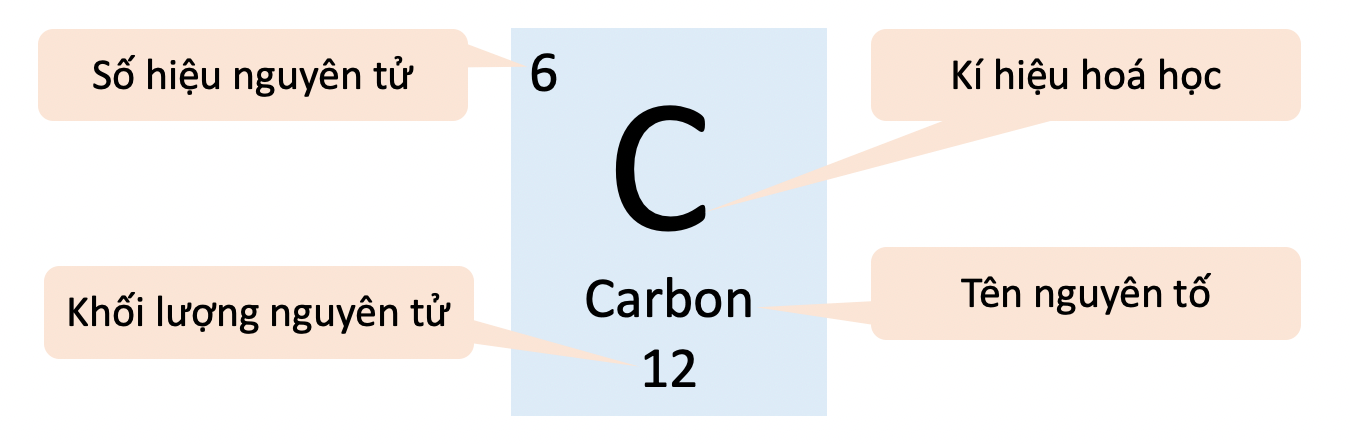 - Ô yếu tắc mang đến biết:
- Ô yếu tắc mang đến biết:
+ Số hiệu vẹn toàn tử (Z).
+ Kí hiệu hoá học tập.
+ Tên yếu tắc.
+ Khối lượng vẹn toàn tử.
- Số hiệu vẹn toàn tử (Z) = số đơn vị chức năng năng lượng điện phân tử nhân = số electron vô vẹn toàn tử = số trật tự của yếu tắc vô bảng tuần trả.
2. Chu kì
- Chu kì bao gồm những yếu tắc tuy nhiên vẹn toàn tử của bọn chúng đem nằm trong số lớp electron và được bố trí trở thành sản phẩm theo dõi năng lượng điện phân tử nhân tăng dần dần kể từ trái khoáy qua loa nên.
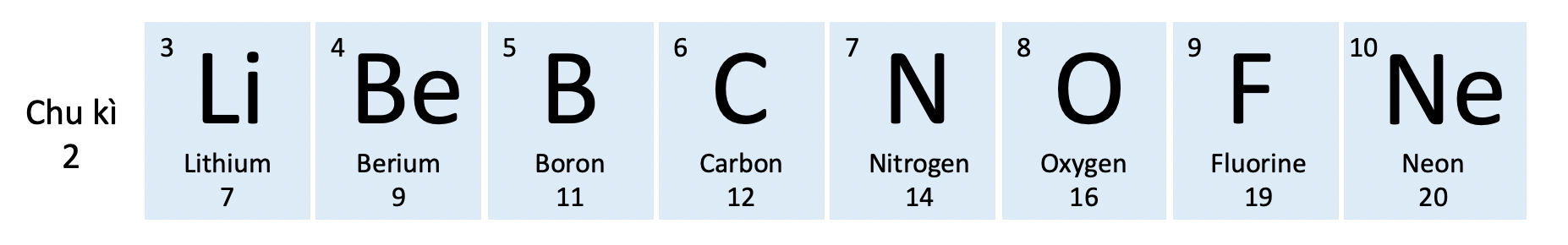 Chu kì 2 vô bảng tuần trả những yếu tắc hoá học
Chu kì 2 vô bảng tuần trả những yếu tắc hoá học
- Bảng tuần trả lúc bấy giờ bao gồm 7 chu kì, được viết số từ một cho tới 7.
- Chu kì 1, 2, 3 được gọi tà tà những chu kì nhỏ, chu kì 4, 5, 6, 7 được gọi tà tà những chu kì rộng lớn.
Ví dụ 2: Chu kì 1 bao gồm nhị yếu tắc H và He, chu kì 2 bao gồm 8 yếu tắc kể từ Li cho tới Ne, chu kì 3 bao gồm 8 yếu tắc kể từ Na cho tới Ar.
3. Nhóm
Xem thêm: giải pháp bảo vệ môi trường
- Bảng tuần trả bao gồm 8 group A được viết số kể từ IA cho tới VIIIA và 8 group B được viết số kể từ IB cho tới VIIIB.
- Các yếu tắc vô và một group A đem số electron phần ngoài nằm trong tương đương nhau, vì thế bọn chúng đem đặc thù hoá học tập tương tự động nhau.
- Trong và một group, khi lên đường kể từ bên trên xuống bên dưới, năng lượng điện phân tử nhân tăng dần dần.
- Số trật tự của tập thể nhóm A ngay số electron phần ngoài nằm trong vô vẹn toàn tử của yếu tắc nằm trong group cơ.
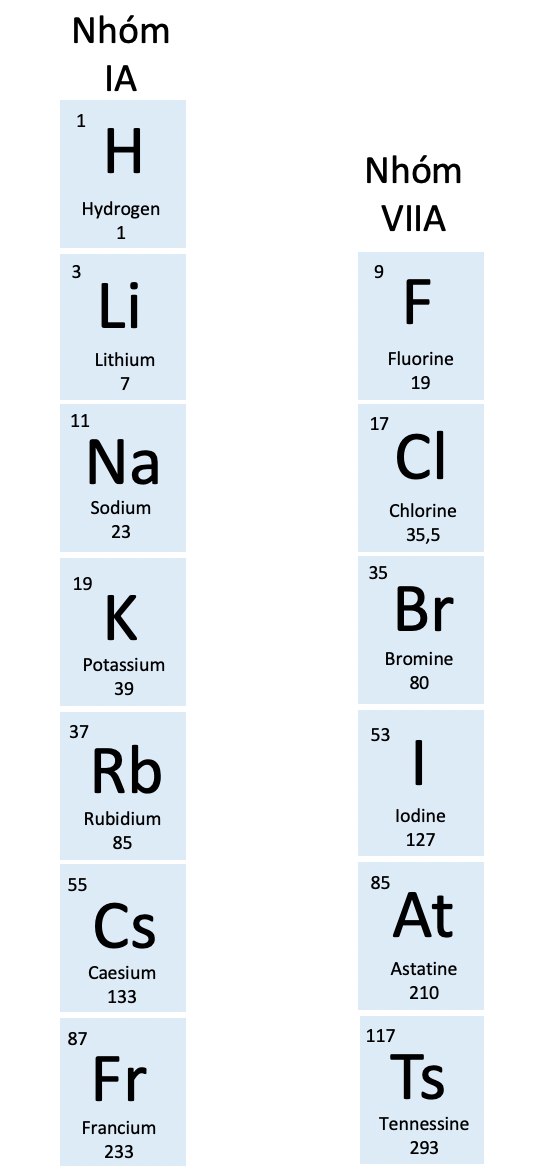
Nhóm IA và VIIA vô bảng tuần hoàn
III. Vị trí những group yếu tắc sắt kẽm kim loại, phi kim và khí khan hiếm vô bảng tuần hoàn
1. Các yếu tắc kim loại
- Trong số 118 yếu tắc hoá học tập tiếp tục biết đem rộng lớn 90 yếu tắc sắt kẽm kim loại.
- Vị trí yếu tắc kim loại trong bảng tuần hoàn:
+ Hầu không còn những yếu tắc nằm trong group IA, IIA, IIIA và một trong những yếu tắc ở những group IVA, VA, VIA.
+ Các yếu tắc nằm trong group IB cho tới VIIIB, những yếu tắc lanthanide và actinide ở cuối bảng tuần trả.
 Ứng dụng của một trong những yếu tắc sắt kẽm kim loại thông thườn vô đời sống
Ứng dụng của một trong những yếu tắc sắt kẽm kim loại thông thườn vô đời sống
2. Các yếu tắc phi kim
- Trong số 118 yếu tắc hoá học tập tiếp tục biết đem không tới đôi mươi yếu tắc là phi kim.
- Tại ĐK thông thường, bọn chúng rất có thể ở thể rắn, thể lỏng hoặc thể khí.
- Vị trí yếu tắc phi kim trong bảng tuần hoàn:
+ Hầu không còn những yếu tắc nằm trong group VA, VIA, VIIA.
+ Một số yếu tắc nằm trong group IIIA, IVA.
+ Nguyên tố H ở group IA.

3. Các yếu tắc khí hiếm
- Trong số 118 yếu tắc hoá học tập tiếp tục biết đem 7 yếu tắc là yếu tắc khí khan hiếm.
- Nguyên tử của bọn chúng đem lớp electron ngoài nằm trong bền vững và kiên cố nên khó khăn bị biến hóa hoá học tập.
- Nguyên tố khí khan hiếm nằm ở vị trí group VIIIA vô bảng tuần trả.
Xem thêm: nghị luận về niềm tin trong cuộc sống

Sơ thiết bị tư duy:
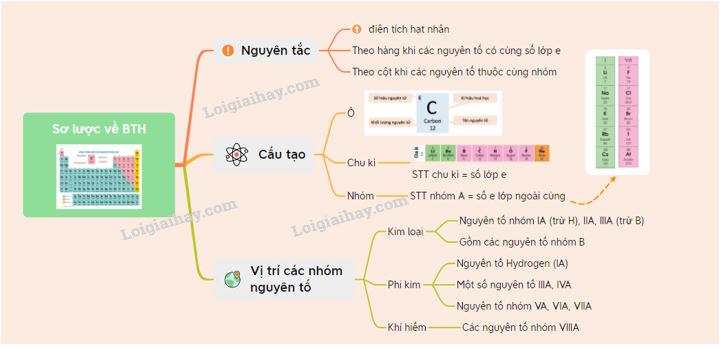












Bình luận